介紹 酸堿滴定 滴定曲線是顯示滴定溶液的pH相對于添加的標準溶液(滴定劑)的體積變化的圖。酸堿滴定曲線可以用幾種方法構建。一種方法是在每次從滴定劑溶液中手動添加等分試樣后手動記錄和繪制pH值。另一種方法是在自動添加滴定劑期間連續(xù)自動記錄和繪制pH值。最后一種方法是昂貴的自動滴定設備的操作原理。DrDAQ數(shù)據(jù)記錄器通過PicoLog數(shù)據(jù)記錄軟件連接到PC允許自動記錄和繪制pH值。可以通過蠕動泵或注射器型泵實現(xiàn)滴定劑溶液的連續(xù)添加,該泵以預定和固定的速率泵送溶液。更便宜的替代方案是使用空氣泵(就像在家庭水族箱中使用的那樣)。這個實驗的目標是多方面的: 1.以與自動滴定儀非常相似的方式構建酸堿滴定曲線。 2.通過使用DrDAQ作為教育工具,了解與酸堿滴定曲線相關的一些原則。 3.使用生成的滴定曲線確定常見樣品中某些分析物的濃度,如:醋中的醋酸和發(fā)酵粉中的碳酸氫鈉。
所需設備
DrDAQ。
玻璃復合pH電極。
一個燒杯(125毫升)。
磁力攪拌器 - 磁棒
空氣泵(JUN ACO 9903)(可證明實驗的有效性)具有更高的準確性和可靠性,優(yōu)選蠕動泵或注射泵。
Tygon管。
1升帶蓋子的玻璃瓶。
0.1 mol / L HCl。
0.1 mol / L NaOH。
0.1mol / L Na 2 CO 3。
尖酸刻薄。
刻度量筒,25毫升。
5毫升刻度移液管。
25毫升移液器。
實驗設置 系統(tǒng)如圖1所示連接。空氣泵以固定且已知的流速推動滴定劑溶液: [滴定劑的體積(V)在時間(t)后加入=流速(mL / sec)*時間(t)(sec)] 通過這種方式,滴定劑的添加量成為時間的線性函數(shù),該變量可以用DrDAQ和PicoLog記錄。
通過修復以下變量,流量保持不變: 泵的速度 控制水龍頭的設置 管道高度高于氣泵水平(這對其他類型的泵來說并不重要)
確保進氣流位于玻璃瓶中的溶液液位之上。不要讓氣泡進入滴定劑溶液。 確保Tygon管周圍沒有空氣泄漏進出玻璃瓶。建議使用環(huán)氧樹脂密封瓶蓋上的管道。 使用高攪拌速率并將玻璃pH電極盡量遠離滴定劑的滴落液,以最大限度地降低玻璃pH電極附近滴定劑的局部濃度。 收集完所有部件后,設置大約需要半小時。 實驗的每個部分需要大約10分鐘,包括在運行之間用蒸餾水洗滌燒杯。
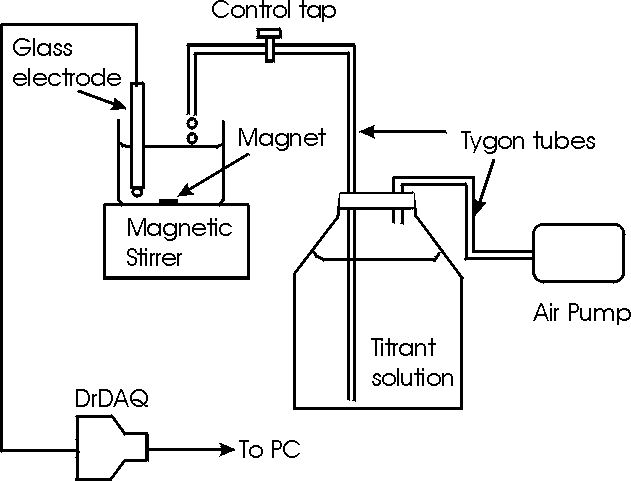
進行實驗 注意:在每次滴定前,記得用蒸餾水清洗反應燒杯和pH電極。 第1部分:設定和確定流速 將25毫升量筒放在管道末端下方。打開空氣泵,在圓筒中收集一定體積(如20 ml)的滴定劑。測量所需的時間(t)。計算流量(F)如下: F = V(ml)/ t(s) 約1-3ml / min(0.0166-0.05ml / sec)的流速是合適的。測量流速后,請勿更改設置。 第2部分:未知HCl濃度的測定(HCl的標準化) 在1升玻璃瓶中加入未知的HCl溶液(~1 mol / l)。 移取5ml 1.0mol / l Na 2 CO 3溶液到125ml玻璃燒杯中。 加入約50毫升蒸餾水。 將玻璃pH電極浸入溶液中。 打開磁力攪拌器。 將PicoLog設置為以每2秒一個樣本的頻率監(jiān)測pH。 同時,用DrDAQ開始記錄并啟動滴定劑流(只需打開空氣泵)。 注意,初始pH是堿性的(碳酸鈉是堿性鹽)。 觀察pH在終點之前的整個間隔內(nèi)如何緩慢下降以及pH在終點附近的非常有限的時間內(nèi)如何突然變化。 在此應用程序中觀察PicoLog自動縮放功能的優(yōu)勢。 請注意,曲線以相等的時間間隔顯示兩個pH值下降(添加相同的體積)。 測量完全中和碳酸鈉所需的時間(t)(第二個終點)。 從以下表達式計算HCl溶液的摩爾濃度(M): M (HCl) = [(M×V)碳酸鹽 ×2] / [(t×F)] 這種設置與商用自動滴定儀幾乎相同,后者具有以下集成系統(tǒng): 提供滴定劑, 監(jiān)測pH值, 繪制曲線和 檢測終點。 自動滴定儀具有復雜的機制,允許可變流速,以獲得更精確的終點位置。 第3部分:測定氫氧化鈉溶液的濃度 將5ml未知的氫氧化鈉溶液吸移到125ml玻璃燒杯中。 加入約50毫升蒸餾水。 使用前一部分中使用的相同HCl。 重復上述步驟。 注意,起始pH非常高(強堿) 僅觀察到一次大的pH跳躍。 找到終點的時間(t)(在這種情況下,曲線中最陡的點對應于pH 7)。(PicoLog光標將幫助您定義終點。) 從以下表達式計算NaOH溶液的摩爾濃度(M) M (NaOH) = [M (HCl) ×(t)×F] / V (NaOH) 第4部分:商業(yè)發(fā)酵粉中碳酸氫鈉含量的測定 將5克發(fā)酵粉懸浮在100毫升蒸餾水中。 搖勻并用50ml等分試樣移入125ml玻璃燒杯中。 使用相同的HCl溶液如上所述滴定。 注意,碳酸氫鹽溶液的初始pH值比第2部分中描述的碳酸鹽溶液的初始pH值低得多(~7.2)。 碳酸氫鈉的%(w / w)由以下表達式計算: 碳酸氫鈉%(w / w)= [(M (HCl) ×t×F×84×2]×100/5 第5部分:醋中乙酸含量的測定 在玻璃瓶中加入第3部分中確定的NaOH溶液,用作滴定劑。 校準流速(F)。 將10ml商業(yè)醋移液到125ml玻璃燒杯中。 用約50毫升蒸餾水稀釋。 重復上述步驟。 觀察到初始pH值處于酸性區(qū)域。這是由于醋中存在乙酸。 從以下表述計算乙酸的%濃度: %(w / w)= [(M (NaOH) ×F×t×60.05×10] / 1000 第6部分:乙酸和HCl與NaOH滴定的比較: 移取在125ml燒杯中的部分2-4中使用的10ml等份的HCl溶液。 用約50毫升蒸餾水稀釋。 重復第5部分。 觀察到初始pH值處于酸性區(qū)域并且僅發(fā)生一次pH跳躍。
查看結果